Biosyntesen af histidin |
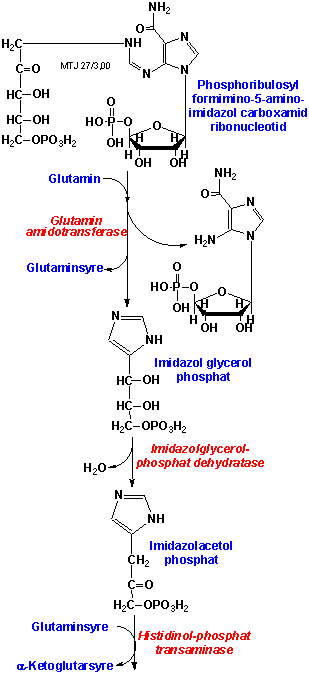
Biosyntesen af den essentielle aminosyre histidin starter med at 5-Phosphoribosyl 1-pyrophosphorsyre kobles med ATP og danner N1-(5'-phosphoribosyl)-ATP, denne forbindelse mister en pyrophosphatenhed og danner N1-(5'-phosphoribosyl)-AMP, derefter sker der en ringbrydning i adeninringen ved hydrolyse og forbindelsen phosphoribosyl formimino-5-aminoimidazol carboximid ribonucleotid dannes som igen isomeriserer til phosphoribolusylformimino-5-aminoimidazol carboximid ribonucleotid.. Ved at modtage en aminogruppe fra glutamin (som omdannes til glutaminsyre) og ved at fraspalte resterne af ATP-molekylet dannes imidazol glycerolphosphat. Denne forbindelse mister vand og danner imidazol acetolphosphat som igen ved transaminering med glutaminsyre (som omdannes til α-ketoglutarsyre) danner L-histidinolphosphat. Forbindelsen fraspalter phosphatgruppen og danner L-histidinol. Hydroxygruppen oxideres derefter i to trin (af det samme enzym - histidinol dehydrogenase) ved NAD+ til en carboxylsyregruppe og L-histidin er dannet. De sidste to trin hvor en alkoholgruppe oxideres til en carboxylsyregruppe er ret usædvanlige idet carboxylsyregruppen hos de fleste andre aminosyrer har sin oprindelse fra en α-ketosyre. Det første trin i reaktionssekvensen katalyserers af det allosteriske enzym, ATP phosphoribosyl transferase, som hæmmes af reaktionsekvensens produkt: Histidin, et eksempel på feedbackhæmning.


BioSite 27/3,00; 10/8,02